Culturing, Visualizing, and Perturbing Cells
차례
Cell Culture
Cell culture시 필요한 것들
- 필수: 온도, pH, 이온조성, 영양분, Culture Dish (coated)
- 선택: Antibiotics, Clean bench
Cell culture medium의 조성
- 필수 아미노산 9가지: phenylalanine, valine, threonin, tryptophan, isoleucine, methionine, leucine, lysine, histidine
- 추가 아미노산 3+1가지: cysteine, tyrosine, arginine + glutamine
- 기타: vitamins, salts, fatty acids, glucose
- Serum: insulin, transferrin, growth factors
Primary Cell Cultures
Cell Preparation
Cell adhesion molecule 떼기: trypsin, collagenase, Ca2+ chelator (EDTA), Ca2+-free medium (교과서 20장)
- Fibroblasts: 너무 잘 자라서 주의해야 함
- Cell senescence: 예) human fetal fibroblasts는 약 50번 분열 후 멈춤
- Embryonic stem cell은 계속 분열함 (교과서 21장)
- 적절한 passage에서 질소통에 얼려두고 다시 녹여 쓰자
- 일부 세포는 senescence stage에 들어가지 않고 oncogenic transformation이 됨 (immortalized cell line)
Immortalized Cells
HeLa cell line: from cervical cancer cells (1951.02.08) from Henrietta Lacks (1951.10.04 사망)
Chinese hamster ovary cell (CHO cell): epithelial cell line derived from the ovary of the Chinese hamster (Theodore T. Puck's lab, 1957)
HEK 293 cells: from human embryonic kidney cells (Alex van der Eb's lab, Leiden, the Netherlands, 1973)
FACS
Fluorescence Activated Cell Sorting (FACS)
3D culture
Culture dish에 키우는 세포는 실제 in vivo 환경을 정확히 재현하지 않는다.
- 예시: Epithelial Cells (20장에서 자세히 나옴)
- basal surface가 extracellular matrix (basal lamina)에 접해있음
- apical surface와 basal surface에서 발현 단백질이 완전히 다르고,
- 이 두 surface간의 물질 이동이 epithelial cell의 주요 기능이다.
- 즉, 세포를 culture dish에 키우면 이러한 기능이 발현되지 않는다.
- 구멍 뚫린 membrane 위에 키우면 세포가 이를 ECM으로 인식한다.
- Madin-Darby canine kidney (MDCK) cells: Epithelial sheets의 형성과 기능 연구에 많이 쓰는 cell line
- 2차원 평면에 키우면 실제 생리적인 환경과 많이 다름
- 적당한 환경에서 키우면 apical과 basal 쪽이 구분되는 tubular sheet 구조가 관찰됨.
- Madin-Darby canine kidney (MDCK) cells: Epithelial sheets의 형성과 기능 연구에 많이 쓰는 cell line
Hybridoma
Monoclonal Antibody Production
- Immunization of Mice and Selection of Mouse Donors for Generation of Hybridoma Cells
- Screening of Mice for Antibody Production
- Preparation of Myeloma Cells(immortal lymphocytes)
- Fusion of Myeloma Cells with Immune Spleen Cells
Selection & Cloning of Hybridoma Cell Lines
광학현미경
Resolution: 두 물체를 둘이라고 구분할 수 있는 최소 거리
- ƛ: wavelength
- n: refraction index of medium. 대략, oil 1.56, 물 1.3, 공기 1.0
- θ: 입사각. lens와 표본이 가까울수록 커짐
- NA: numerical aperture
- 좋은 렌즈는 resolution이 좋다. (maginification은 중요하지 않음)
좋은 렌즈의 NA > 1.4, 아주 좋은 렌즈의 NA > 1.7
- 현존하는 최고 렌즈의 가시광선 resolution은 대략 0.2 µm
- 그러나 antibody를 이용하여 gold particle을 붙히고 컴퓨터로 보정하면 광학 현미경이라도 5 nm resolution 이미지 취득가능 (그림 17-29, 17-30 참고)
참고자료:
MicroscopyU: Nikon에서 운영하는 현미경 종합 설명 세트

위상차 현미경, DIC 현미경
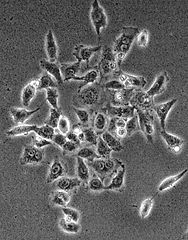
위상차 현미경
- 1934 네덜란드 물리학자 Frits Zernike가 개발
시편을 통과하는 light wave의 위상차를 amplitude로 바꾸는 장치 -> 두께가 밝기로 전환되서 보임
Differential Interference Contrast 현미경 (Nomarski Optics)
- 1952 Georges Nomarski가 위상차 현미경을 개선해서 개발
- DIC 현미경은 렌즈의 NA를 손해보지 않고 모두 사용함
- 위상차 현미경은 light source가 얇은 막 형태: 광량에 한계가 있음
위상차 현미경은 시편이 매우 얇아야 함 -> DIC는 두꺼운 조직도 관찰 가능
위상차 현미경은 시편 뒤에 halo가 생김 -> DIC는 안 생김
- 원리:
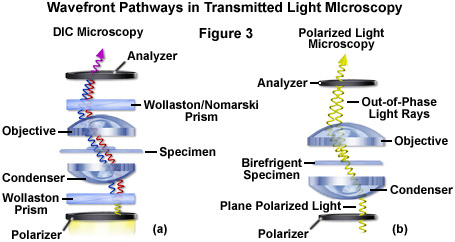
- Light source를 편광으로 만든 후, two-layered modified Wollaston prism을 통과시켜 두 light path로 나눔
- 두 light path 중 하나는 시편을 통과하고, 하나는 시편을 통하지 않고 그대로 통과시킴
- 두 light path는 대물렌즈를 통과 후 upper Wollaston prism 에 의해서 하나로 모아짐
- 이 때 시편의 두께와 refractive index에 따라 light wave의 상쇄가 일어나 상이 입체로 보임

- 참고: 그림 9-8b, 그림 9-9
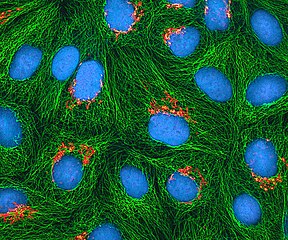
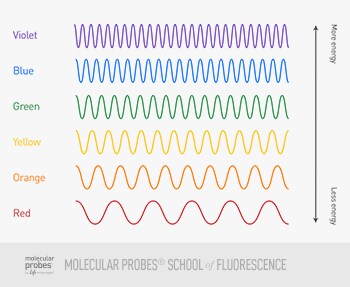
형광 현미경
Immunofluorescence Antibody

- Direct (Conjugated Ab): 쉽고 비쌈. Ab+형광 파장 조합을 다 구매해야 함.
- Indirect (1st + 2nd Ab): Step 복잡. Ab 사용에 융통성 있다. 2ndary Ab 붙힐 때 시그날 증폭됨.

- Fura-2 단독으로는 340 nm excitation일 때 510 nm emission 이 가장 세다
Fura-2+Ca2+ chelation되면 380 nm excitation일 때 510 nm emission 이 가장 세다
- 340nm 파장과 380nm 파장으로 excitation 시킨 후, 510 nm 파장대의 세기를 측정해서 그 비율을 구하면 세포내 칼슘 농도를 측정할 수 있다. (dual excitation, single emission)
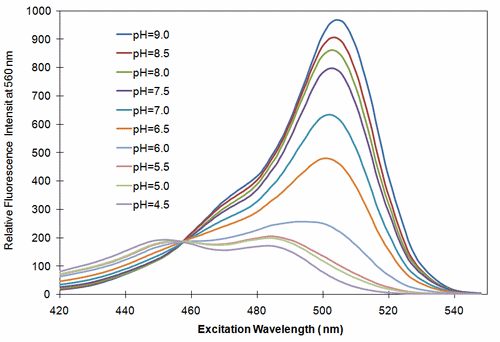
- Fura-2와 비슷한 dual excitation, single emission system 필요
- 440 nm와 490 nm로 excitation 시키고, 535 nm 파장의 세기를 측정해서 pH 측정
Confocal Microscopy
형광 현미경의 단점: 시편 내의 모든 형광 물질이 light source가 된다.
- 해결책1: 보고자하는 focal plane 위 아래에 맺힌 out of focus 형광 상을 제외 (computerized decovolution)
- 해결책2: 보고자하는 focal plane 외의 상은 모두 걸러낸다 (confocal microscopy)

Total Internal Reflection (TIRF) Microscopy
Coverslip에 인접한 부위(100 nm 이내)만 excite 시키는 방식
- Microtubules, actin filaments등 coverslip에 인접한 세포 구조 관찰 시 유리

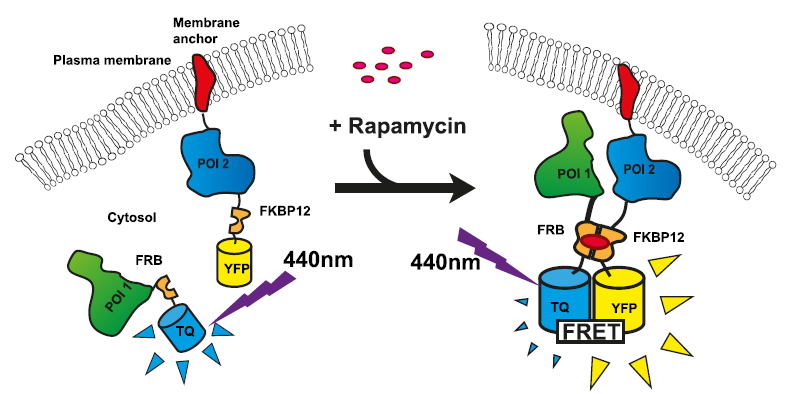
Förster resonance energy transfer (FRET)
형광물질1의 emission이 형광물질2를 excite 시키는 방식

- 두 단백질이 인접해서 작동하는지를 보여줌
전자현미경
Resolution: 두 물체를 둘이라고 구분할 수 있는 최소 거리
- ƛ: wavelength
- n: refraction index of medium. 대략, oil 1.56, 물 1.3, 공기 1.0
- θ: 입사각. lens와 표본이 가까울수록 커짐
- NA: numerical aperture
Electron의 wavelength = 1.23 nm (가시광선은 400~750 nm)
- 이론적 resolution은 대충 0.005 nm, 실제로는 0.1 nm 가량
TEM vs. SEM (Transmission vs. Scanning electron microscope)
- Nagative Stain

- 구리나 금 Grid에 샘플 놓고, heavy metal incubation 후 샘플 제거
- 샘플이 없는 곳만 heavy metal로 staining 되고, 상으로 나타남 (negative image)
- Metal Shadowing
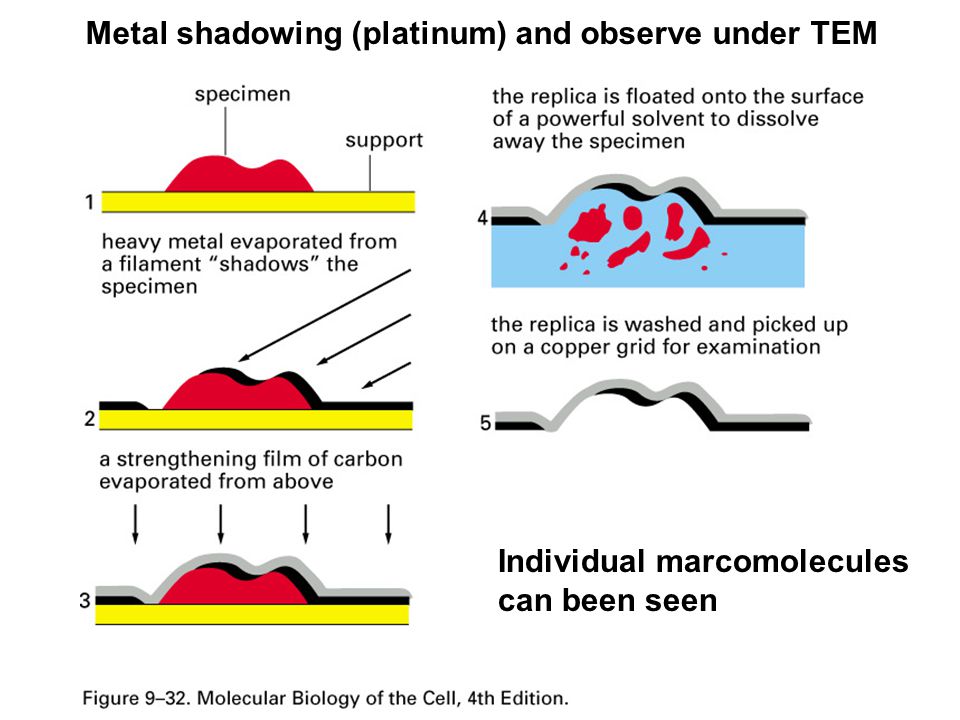
- 3차원 이미지 취득 가능
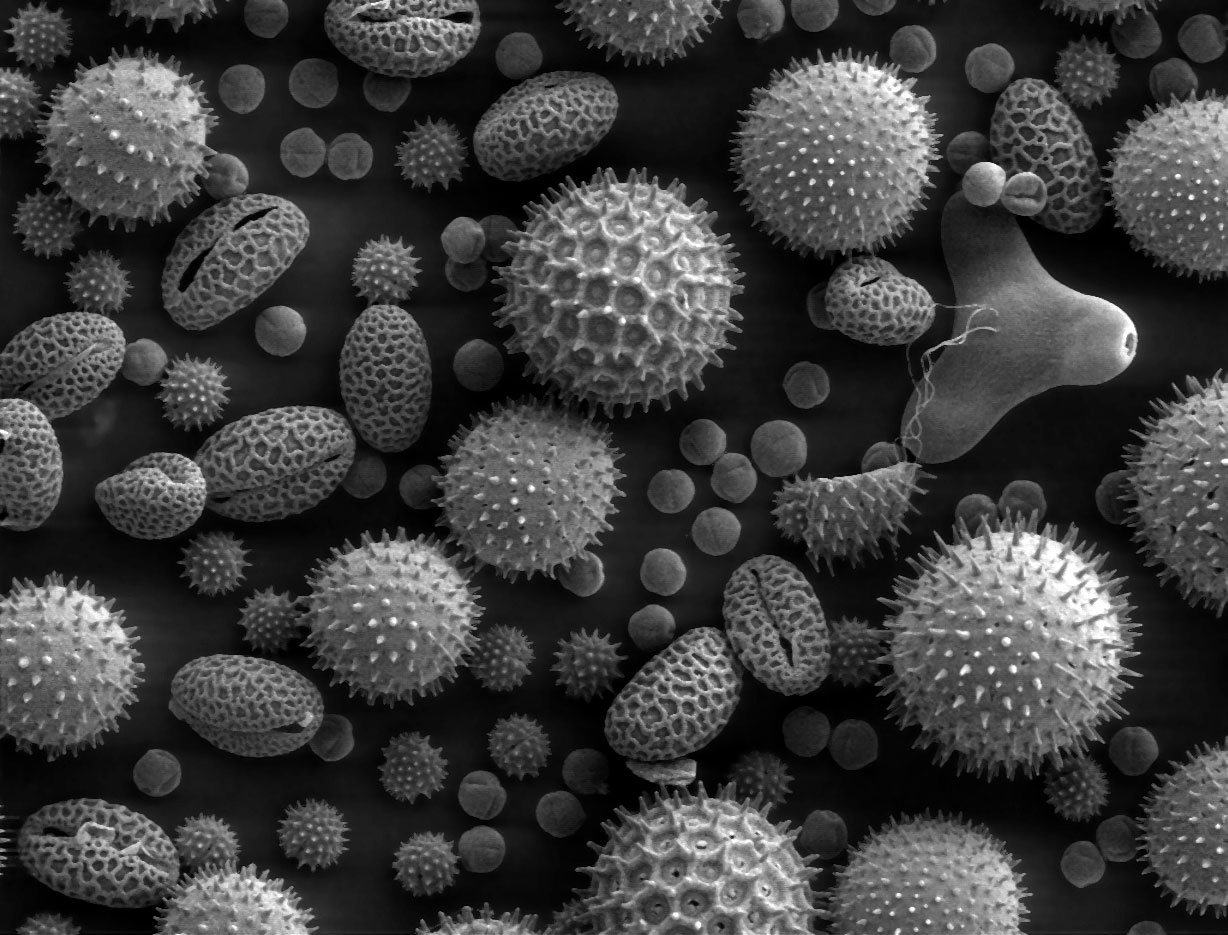
- unsectioned metal-coated 시료의 표면 관찰가능
시료 표면의 heavy metal이 2차 전자를 방출하여 음극관에 붙음 -> 브라운관 TV와 같은 원리
- 3차원 영상으로 관찰 가능하지만, resolution이 10 nm 가량으로 TEM에 비해 떨어짐
세포 소기관 보기
세포 기능 조절
Gain of function tests vs. Loss of function tests
약물
예시) 16,320개의 약물 중 mitosis inhibitor가 무엇인지? (T.U.Mayer. 1999 Science)
- mitotic stage에서 멈춘 세포를 증가시키는지 mitosis marker로 screening: 139개로 추려짐
tubulin 관련 drug는 mitotic spindle의 생성에 영향을 주지만 mitosis에 직접 영향을 미치지 약물은 아니므로 제외: 139 -> 86개로 압축
- 86개의 약물을 적용 후 microtubules, actin, chromatin을 형광현미경으로 관찰하여 mitosis 시기에만 영향을 미치는 후보물질 5개 선정
그 5개의 약물중 하나가 monastrol임 (spindle의 bipolar localization을 방해함)
Small interfering RNA
- Target mRNA에만 있는 ~21 bp sequence 선정
- dsRNA 제작 후 적용
- 24~72 시간 후 protein 정량 (immunoblotting)
- siEBP50 (D.윗줄) vs. siGL2 (D.아래)
C.elegans
| /Ch09 /Ch11 |