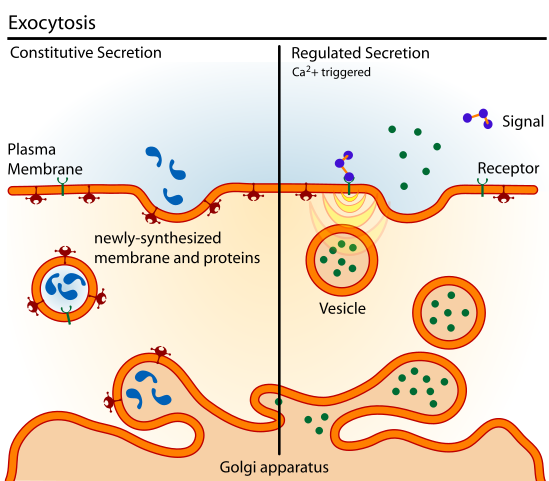
Transmembrane Transport of Ions and Small Molecules
차례
확산
 픽의 확산법칙: 확산 J는 확산계수 D와 밀도 차 ∂n에 비례, 거리 차 ∂x에 반비례
픽의 확산법칙: 확산 J는 확산계수 D와 밀도 차 ∂n에 비례, 거리 차 ∂x에 반비례
- 세포막을 사이에 둔 확산의 경우, 확산계수, 밀도차, 지질 용해도에 비례, 거리(세포막두께)에 반비례
통로(Channel)
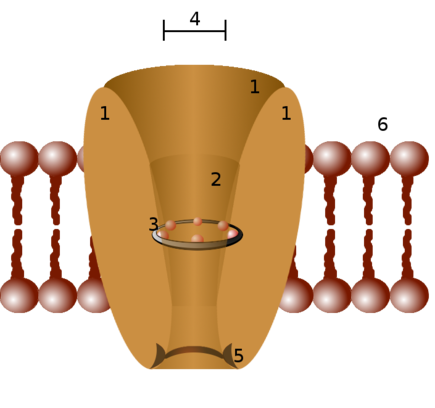 세포막단백질의 종류. 수용성 물질을 통과시킨다.
세포막단백질의 종류. 수용성 물질을 통과시킨다.
- Voltage-gated, Ligand-gated, Mechanically-gated 등
촉진확산(Facilitated diffusion)

운반체 역할을 하는 세포막단백질에 붙어서 확산 이동
- Channel과 다른점
- 운반체에 binding을 한다는 점에서 channel과 다름
- 확산 속도가 Saturation 됨. (채널을 통한 확산은 오로지 농도차에 비례)
예: glucose (Glut4), amino acid 등
- 동의어: facilitated transport, passive-mediated transport
능동수송
Active transport: 농도 경사에 따라 이동하는 확산과 달리, 농도 경사를 거꾸로 이동함. 에너지(ATP) 필요함.
1차 능동수송: Na+-K+ pump (Na+/K+-ATPase), Ca2+ pump (Ca2+-ATPase), H+ pump (H+-ATPase)
예시: ATP 한 분자를 hydrolysis 하여 3 Na+를 세포 밖으로 퍼내고, 2 K+를 세포 안으로 들여온다 (Na+-K+ pump)

- 2차 능동수송: 1차 능동수송에 의해 생긴 농도 경사를 이용하여 물질을 이동 시킨다.
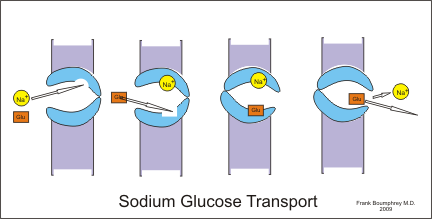
Symport (같은 방향): Na+-K+-2Cl- co-transporter, Sodium-glucose transport proteins
Antiport (역방향): Na+-Ca2+ exchanger
Ion Channels
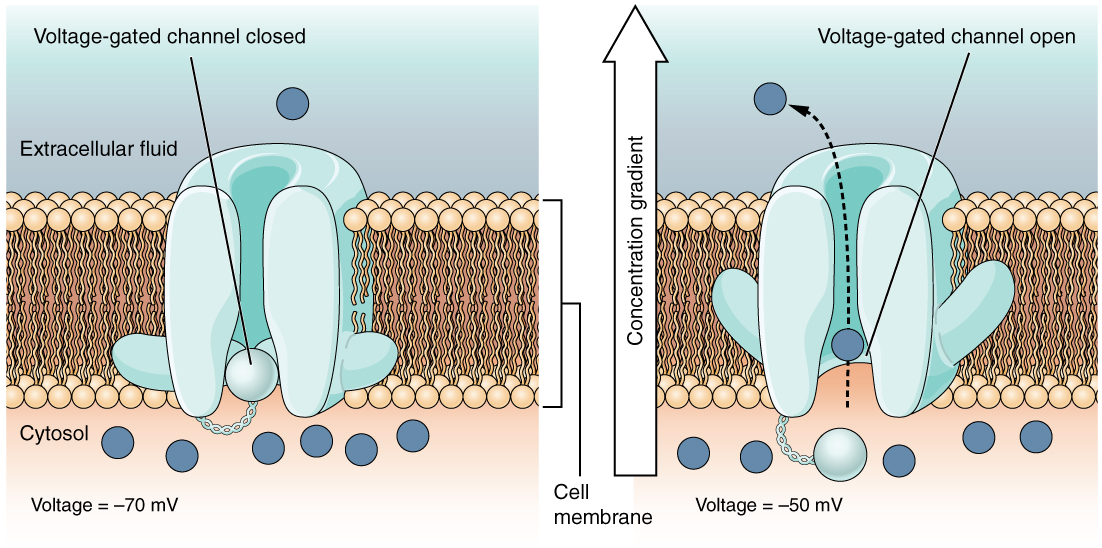
- 막 단백질 (Transmembrane Protein)
- 이온의 수동적 확산(passive diffusion)의 통로 ➔ 이온의 이동을 유발하지는 않음
- Ion Selectivity: 특정 이온만 선택적으로 통과시킴
- Permeability: 이온의 투과도 (이온이 얼마나 쉽게 통과하나)
- Gating: 특정 조건에서 permeability가 달라짐 (channel이 열리고 닫히는 조건 있음)
이온의 이동
Ion channel이 열려도 (=permeability가 증가해도), 이온이 이동할지 말지는 이온이 정한다. 이 때 이온은 두 가지를 고려해서 거취를 정한다.
- 확산(diffusion): 농도가 높은 곳에서 낮은 곳으로 이동하려고 한다 (=확산의 정의)
- "농도경사(concentration gradient)에 따라 이동한다"라고 한다.
- 전하의 종류: 같은 종류의 전하끼리를 배척하고, 다른 종류의 전하끼리는 붙는다.
- "전기적 경사(electrical gradient)에 따라 이동한다"라고 한다.
깁스-도난 평형
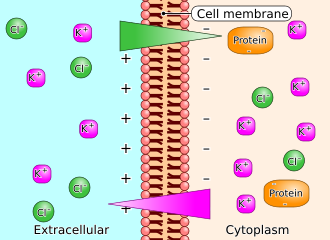
- 세포 안에는 단백질이 많은데, 단백질은 크기가 커서 세포막을 통과 못 한다.
- 단백질은 음전하를 띄고 있어서 양이온을 끌어모으고,
- 양이온의 이동은 음이온의 이동을 유발하여,
세포안에는 세포밖보다 더 많은 particle이 있게 된다. ➔ 이 상태를 Gibbs–Donnan effect라 부른다.
양이온 X+, 음이온 Y-
세포외액
세포내액
초기값
9 X+, 9 Y-
9 X+, 3 Protein3-
평형상태
6 X+, 6 Y-
12 X+, 3 Y-, 3 Protein3-
Particle 수 (삼투압 발생)
12 particles
18 particles
- 세포막 안팎의 삼투압 평형이 맞을 때까지 물이 세포 안으로 계속 들어오면 세포막이 터질 것이나,
세포안의 초과 X+를 세포외로 꾸준히 내보냄(Na+-K+ pump)으로써 삼투압 불균형과 물의 이동을 제한하여
- 실제로는 터지지 않는다.
Nernst Equation
Gate가 열렸고, 다음 조건이 맞으면 이온은 이동한다.
- 농도경사와 전기적 경사의 방향이 같다면 그 방향으로 이동한다.
- 농도경사와 전기적 경사를 한꺼번에 편의상 electrochemical gradient라고 부른다.
- 이온의 이동(ionic current)은 편의상 전류(電流, electric current)와 동의어로 취급한다.
- 농도경사와 전기적 경사의 방향이 다르다면, 그 둘 사이에서 평형점으로 이동한다.
- 이동의 결과 농도가 달라지면 새로운 평형점이 생긴다.
Electrochemical gradient의 평형점은 1887년 23살의 Walther Nernst가 찾음 (후에 노벨상 받음).
- 현재 세포 안팎의 전압차가 equilibrium potential과 같다면 이온이 이동할 이유가 없다 (딱 그 농도가 좋은 상태)
- 현재 세포 안팎의 전압차가 equilibrium potential과 다르다면 이온의 전하에 따라 이동의 방향이 결정된다.
Nernst Equation Simulator for Mac/Windows/Web(Flash 필요, Chrome 안됨)
연습문제: 가상의 양이온 X+의 세포내 농도가 150 mM, 세포외 농도가 5 mM 이라면 X+의 equilibrium potential(EX)는?
답은 여기에 (온도는 310°K 라고 가정)
Goldman-Hodgkin-Katz Equation
- Nernst Eq.는 한가지 이온의 농도차와 그 이온의 equilibrium potential과의 관계를 보여주는데, 실제 상황에서 한가지 이온만 존재하는 경우는 없다.
여러가지 이온이 혼재할 때 equilibrium potential은 1943년 David E. Goldman이 박사학위 논문으로 발표함
Nernst Eq.과 다른점: 그 이온의 농도에 permeability를 곱함. 예를 들어 Na+, K+, Cl-가 있다면,
Goldman-Hodgkin-Katz Equation의 다른 두명은 Alan Lloyd Hodgkin(1963 노벨상)과 Bernard Katz(1970 노벨상).
Goldman Equation Simulator for Mac/Windows/Web(Flash 필요, Chrome 안됨)
Resting Membrane Potential
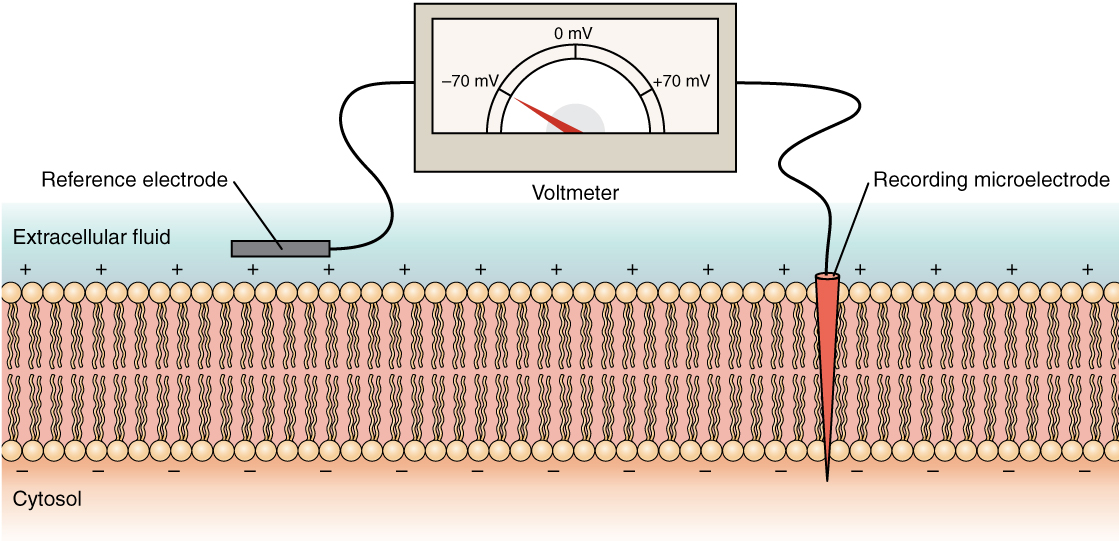
세포막 안팎의 전압차:
- 신경세포라면 -70 mV ~ -60 mV 가량 (신경세포가 아니라면 -90 mV ~ -20 mV 다양함)
- 이온의 permeability 차이 때문에 발생
at Steady State
Imembrane = INa + IK = 0
Imembrane = (Vmembrane - ENa) / RNa + (Vmembrane - EK) / RK = 0 (Ohm's law
)
Vmembrane = (ENa⋅RK + EK⋅RNa) / (RK + RNa)
RNa >>> RK 인 경우, Vmembrane = EK에 근접
RNa <<< RK 인 경우, Vmembrane = ENa에 근접
Vmembrane = (EK⋅GK + ENa⋅GNa) / (GK + GNa)
혹은, Conductance G = 1 / R (저항의 역수) 개념으로 식을 다시 써도 마찬가지,
GNa <<< GK 인 경우, Vmembrane = EK에 근접
GNa >>> GK 인 경우, Vmembrane = ENa에 근접

則, Vmembrane ∝ GNa / GK
at Resting Neuron
일부 K+ channel은 열려 있고 Na+ channel은 닫혀 있다.
GNa <<< GK 하다 (RNa >>> RK)
則, VrestingMembrane = EK에 근접하다.
EK = -90 mV
[K+]OUT / [K+]IN = 5 mM / 150 mM 가정시, Nernst Eq.
왜 [K+] 농도는 세포 내부에 더 높은가? 답: Cytosol에 Anions가 많다.
- 그러나 실제로 Resting Membrane Potential은 -70 mV ~ -60 mV 가량
INa = (Vmembrane - ENa)⋅GNa 에서
Vmembrane과 ENa의 차이가 워낙 크다 (ENa = 대략 +63 mV).
아주 작은 GNa 라도 의미 있는 INa가 발생한다.
이렇게 세포내로 유입되는 INa는 Na+/K+ pump가 상쇄시킨다.
1 ATP를 사용하여 3 Na+를 세포 외로 보내고 2 K+를 세포 내로 유입시키면서 Vmembrane을 -5 mV 가량 더 낮춘다.
세포막을 통과하지 않는 물질이동